En milieu basique non nucléophile et fort , on peut réaliser la transformation suivante :
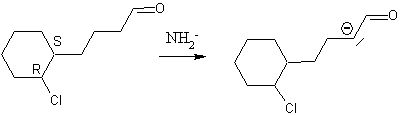
1/ Représenter en perpective les deux conformations possibles de l'ion obtenu . Quelle est la conformation la plus stable ? Quelle est la conformation qui permet une SN2 intramoléculaire?
2/ Représenter en perspective la molécule obtenue à l'issue de la SN2 intramoléculaire, dans la conformation de votre choix. En préciser la configuration.
L'action d'un réducteur tranforme le groupe carbonyle en alcool primaire. Cet alcool est alors transformé en dérivé halogéné par l'action du chlorure de thionyle ou du pentachlorure de phosphore, ou du tribromure de phosphore.
3/ Rappeler le bilan de ces transformations sur un alcool R-CH2-OH .
Le mécanisme, commun à ces trois agents halogénants peut être décrit ainsi :
- L'oxygène de l'alcool , nucléophile, attaque le centre électrophile de l'agent halogénant qui subit une SN2, avec départ d'un halogénure.
- Un proton est alors libéré spontanément de l'intermédiaire acide.
- L'halogène libéré à la première étape joue alors le rôle de nucléophile, sur le carbone électrophile de l'intermédiaire déprotoné, qui subit une SN2, avec départ concerté d'un oxyde et d'un halogénure.
- La réaction ayant lieu en milieu anhydre, le proton libéré à l'étape acido-basique réagit avec la base halogénure, pour former de l'acide halohydrique.
5/ Pourquoi l'action d'un halogénure sur un alcool primaire est-elle sans effet, alors qu'elle est efficace sur l'intermédiaire déprotoné?